現代の都市水環境:人健康、水生生態系への影響の懸念
終戦から1970年代前半までは、戦後の復興に伴う都市人口の増加や経済成長に伴う有機物や重金属汚染の拡大が水汚染の原因でした。いわゆる‘公害’です。公害の時代では、工場排水や農薬による漁業被害、し尿による飲料水源汚染による感染症の蔓延が問題となっていました。公害対策基本法や水質汚濁防止法、化審法等の法整備や下水道、上水道の普及によって公害型の水汚染は克服されてきました。
図1 水環境を取り巻く衛生上の問題の変遷:複雑化/多様化
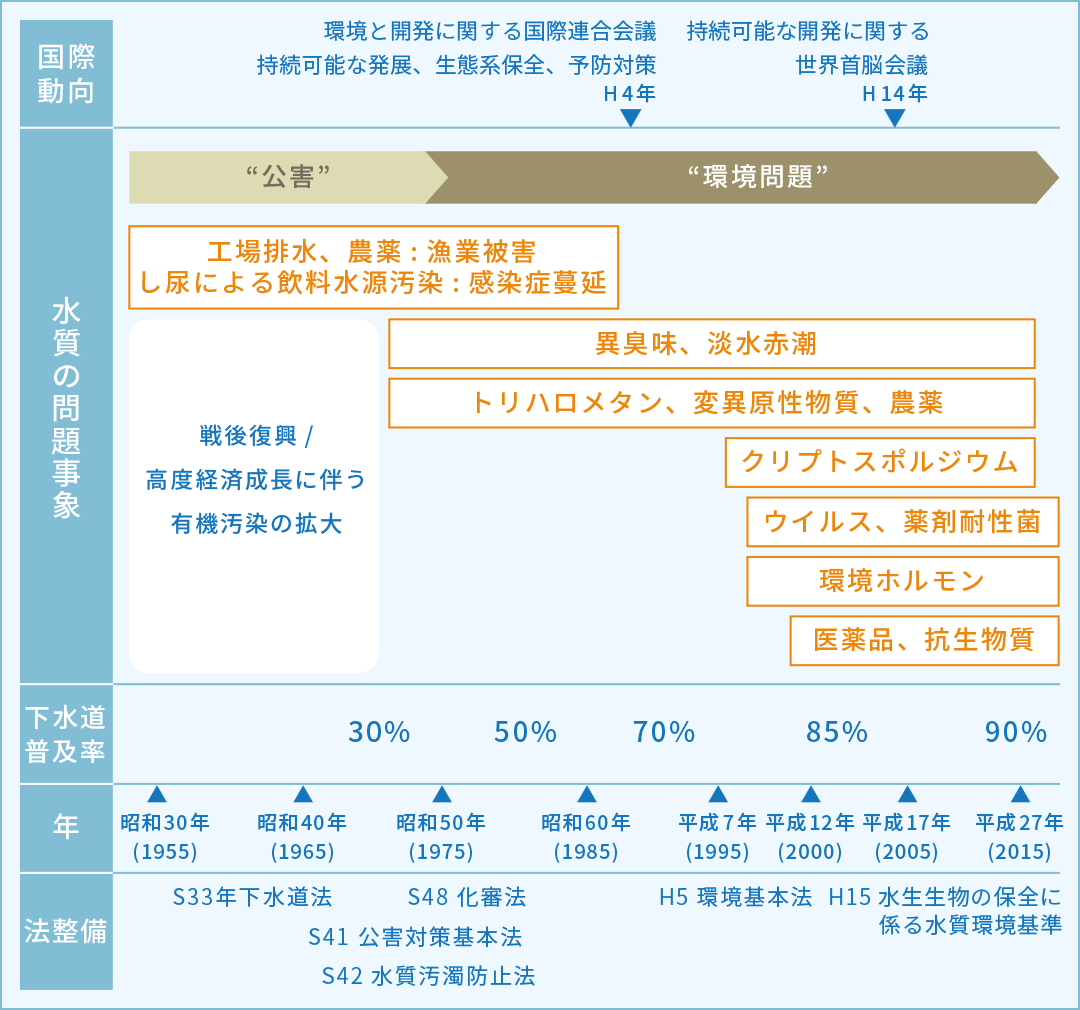
1980年代になると、水汚染は‘環境問題’として捉えられるようになります。その理由は、汚染の原因が工場排水などに代表される経済活動から人間の日常生活に由来する生活排水にシフトしてきたことにあります。また、1992年の環境と開発に関する国際連合会議(リオサミット)に象徴されるように、人健康だけでなく生態系を保全していくことの重要性も認識されるようになりました。環境問題の時代の特徴です。
1990年代半ばになると、水環境中に極低濃度で存在する化学物質が水生生物の生殖器官や繁殖に影響を及ぼすことが明らかとなりました。いわゆる‘環境ホルモン’の問題です。さらに、人が服用した医薬品は屎尿とともに下水処理場へ流入し、下水処理を経た後に河川等の水系へ放出されることが、世界各地で明らかとなってきました。水生生物が長期にわたり医薬品に曝露された場合の悪影響が懸念されます。果たして本当に影響があるのかどうか、その結論が得られるような研究が求められます。
また、Polymerase chain reaction (PCR)法に代表される遺伝子検出技術の進展に伴い、身近な水環境中からもヒト病原性のウイルスが検出されることが明らかとなっています。水環境を取り巻く衛生上の課題は、終戦直後に比べ、より多様化・複雑化してきています(図1)。
図2 現代の都市水環境:人健康、水生生態系への影響の懸念
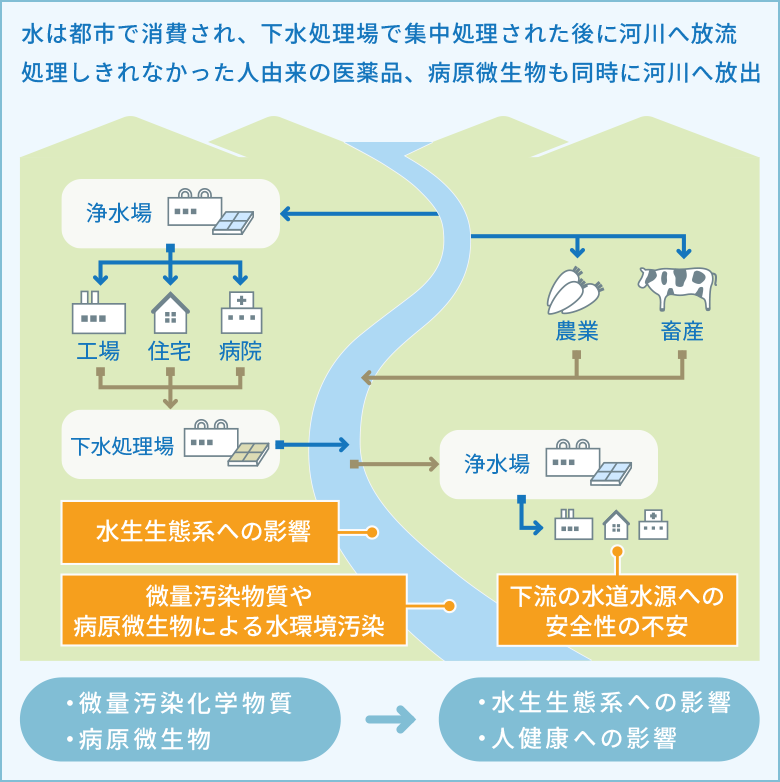
多くの地域で、水は都市で消費され、下水処理場で集中処理された後に河川へ放流されます。下水道の普及とともに下水処理水が放流先水域で水量の面で大きな比率を占める地域が増えています。下水処理場で処理しきれなかった人由来の医薬品も同時に河川へ放出されることになり、放流先河川に生息する水生生物への悪影響が懸念されます。また病原微生物による下流に位置する都市に住む人々の健康影響も懸念されます(図2)。
図3 ヒトの脳で働く神経伝達物質と神経系
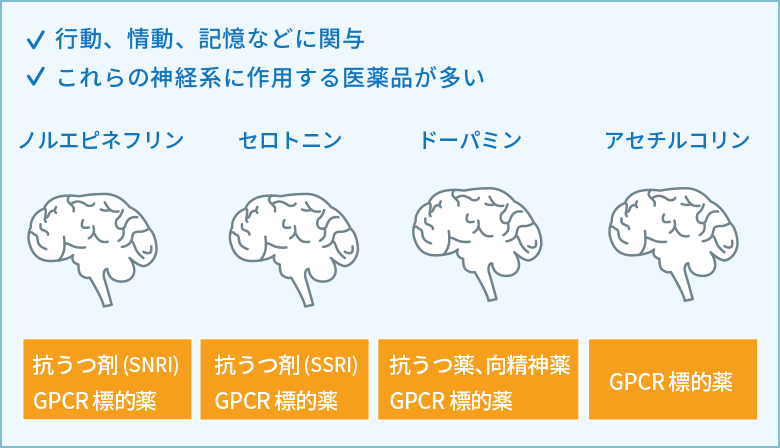
人用の医薬品には、神経系に作用するものが多数あります。例えば、Gタンパク連結型受容体(G protein coupled receptor: GPCR)を標的とした医薬品があります。高血圧の治療薬や、アレルギー性鼻炎の治療薬、咳を鎮めるための薬、胃薬など、様々な種類の医薬品があります。また、日本でも近年処方量の増えている抗うつ薬も神経系に作用する医薬品です。抗うつ薬はセロトニントランスポーター(Serotonin Transporter: SERT)等を標的としています。GPCRやSERTは人だけでなく幅広い生物が保有しているため、GPCR標的型の医薬品や抗うつ薬が水環境中へ放出された場合、水生生物の中枢神経へ作用して悪影響を及ぼすことが懸念されます。実際に、抗うつ薬を魚に曝露すると魚の行動に異常が現れるとの研究結果が多数報告されています。我々は、医薬品の中でも特に神経に作用するタイプの医薬品に焦点をあて、これらの医薬品が水生生物へ与える影響について研究を展開しています(図3)。